Xenotrapianto di cuore, medici e scienziati scrivono le nuove «regole» (e i limiti)
di Ruggiero Corcella (articolo pubblicato dal Corriere della Sera il 6 marzo 2026)
Nel 2000, metteva in guardia: lo xenotrapianto cardiaco – il trapianto di cuore da animale a uomo – era prematuro. Oggi, a distanza di ventisei anni, la nuova Consensus 2026 della International Society for Heart and Lung Transplantation (ISHLT) aggiorna quel giudizio alla luce di progressi genetici e immunologici che hanno portato ai primi due trapianti di cuore suino in pazienti viventi. Il documento è stato pubblicato su The Journal of Heart and Lung Transplantation. Il bisogno resta drammatico: i cuori disponibili per allotrapianto non coprono la domanda. I maiali, opportunamente modificati, rappresentano la fonte più realistica per colmare il divario. Ma la strada è ancora scientificamente complessa.
I criteri fissati nel 2000: quando il traguardo era ancora lontano
Una consensus scientifica si forma quando la maggior parte degli esperti di una disciplina, sulla base di molte evidenze indipendenti e riproducibili, converge sulla stessa spiegazione di un fenomeno. La prima Consensus ISHLT del 2000, richiamata nel documento 2026 , stabiliva paletti molto rigorosi prima di qualsiasi sperimentazione clinica. In particolare, si indicava come soglia minima il raggiungimento di una sopravvivenza di almeno il 60% in un gruppo di almeno 10 primati non umani trapiantati con cuore o polmone suino, con funzione d’organo adeguata per almeno tre mesi e senza complicanze gravi legate a immunosoppressione o infezioni. I candidati umani, inoltre, avrebbero dovuto essere pazienti non eleggibili né a trapianto tradizionale né a supporto meccanico duraturo, oppure con aspettativa di vita troppo breve per attendere un organo umano disponibile. Il documento sottolineava anche la necessità di una stretta supervisione regolatoria nazionale e internazionale, di registri indipendenti per monitorare gli esiti e di una valutazione approfondita del rischio infettivo, inclusa la possibile trasmissione di patogeni suini. A distanza di oltre vent’anni, molte di quelle condizioni restano attuali, a conferma di quanto la prudenza fosse – ed è – parte integrante del percorso verso lo xenotrapianto clinico.
Il nodo immunologico: addomesticare il rigetto
Il principale ostacolo è il sistema immunitario umano, programmato per riconoscere come «estrane» l’organo suino. Il rigetto iperacuto, mediato da anticorpi naturali contro specifici zuccheri presenti sulle cellule del maiale (αGal, Neu5Gc, Sda), è stato in gran parte superato grazie all’ingegneria genetica: i geni che codificano questi antigeni sono stati eliminati nei cosiddetti «triple knock-out».
A ciò si aggiunge l’introduzione di geni umani nel maiale donatoreper regolare complemento e coagulazione – sistemi biologici che, se incompatibili tra specie, possono causare trombosi diffuse e insufficienza dell’organo. Tuttavia, il rigetto anticorpo-mediato tardivo e l’attivazione dell’immunità innata restano problemi centrali.
Per questo la Consensus sottolinea che l’immunosoppressione convenzionale non è sufficiente: il blocco della via CD40/CD154, cruciale nell’attivazione dei linfociti T e B, è considerato cardine terapeutico nei protocolli clinici.
Dai primati all’uomo, cosa abbiamo imparato
Nei modelli preclinici su babbuini, la sopravvivenza dei cuori geneticamente modificati ha progressivamente superato i tre, fino a nove mesi con sistemi di perfusione ipotermica ossigenata. La ISHLT indica come requisito minimo, prima di avviare trial strutturati, almeno 5–10 casi in primati non umani con sopravvivenza di almeno 6 mesi (o maggiore) e funzione d’organo stabile.
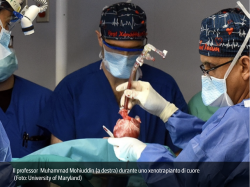
Nei due casi umani eseguiti nel 2022 e nel 2023, entrambi eseguiti dall’equipe con cuori suini modificati con dieci interventi genetici, il rigetto iperacuto è stato evitato. Tuttavia i pazienti sono deceduti rispettivamente a 60 e 40 giorni. Nel primo caso è emersa una possibile riattivazione di citomegalovirus suino (PCMV), nel secondo un rigetto anticorpo-mediato precoce, nonostante bassi livelli di anticorpi anti-suino pre-trapianto. David Bennett Jr, 57 anni, è stato il primo essere umano a sperimentare il trapianto di un cuore di maiale geneticamente modificato, il 7 gennaio 2022 al Centro medico dell’Università del Maryland. A operarlo, il professor Muhammad Mohiuddin.
E, ancora, Lawrence Faucette, 58 anni, il secondo uomo al quale il 20 settembre del 2023 un team dell’Università del Maryland guidato sempre dal professor Mohiuddin aveva impiantato un cuore di maiale geneticamente modificato. Faucette era morto due mesi dopo.
Chirurgia e terapia intensiva: un cuore «diverso»
Il cuore del maiale non è identico a quello umano per orientamento anatomico, dimensioni dei grossi vasi e risposta ai farmaci. È più sensibile alle aritmie e tollera poco le catecolamine. La Consensus raccomanda un controllo pressorio rigoroso per prevenire ipertrofia rapida del’impianto e invita a evitare trasfusioni non selezionate, potenziale fonte di anticorpi anti-suino.
La perfusione continua ipotermica con soluzione ossigenata (Steen) è indicata come tecnica di preservazione di riferimento negli adulti, mentre restano da validare soluzioni alternative in ambito pediatrico.
Sorveglianza immunologica e rischio infettivo
Il monitoraggio non può limitarsi alla biopsia endomiocardica. Si propone l’integrazione con dosaggio del DNA suino circolante, biomarcatori di danno miocardico e test sierologici mirati contro antigeni suini.
Sul fronte infettivo, il rischio non è solo zoonotico in senso stretto (come epatite E o influenza suina), ma anche «xenozoonotico»: virus innocui per l’uomo ma capaci di danneggiare l’organo trapiantato, come il PCMV. Gli allevamenti devono essere «designated pathogen free» e sottoposti a controlli molecolari stringenti. Particolare attenzione è riservata ai retrovirus endogeni suini (PERV), per i quali si raccomanda la selezione di animali PERV-C negativi o strategie di inattivazione genetica.
Chi potrà beneficiarne per primo?
La Consensus suggerisce un percorso graduale. Inizialmente casi «compassionevoli» in pazienti non candidabili a trapianto umano o a supporto meccanico duraturo. Successivamente trial pilota in pazienti anziani, altamente sensibilizzati o con cardiomiopatie non trattabili con altre opzioni.
Nei bambini con cardiopatie congenite complesse lo xenotrapianto potrebbe fungere da «ponte» verso un allotrapianto. Tuttavia la crescita dell’organo suino, anche quando geneticamente modulata, rappresenta una variabile ancora da controllare.
Una roadmap prudente ma concreta
La ISHLT non proclama una rivoluzione imminente, ma definisce una roadmap rigorosa: solide evidenze precliniche, immunosoppressione mirata, sorveglianza integrata e cornici regolatorie coordinate a livello internazionale.
Lo xenotrapianto cardiaco non è più fantascienza, ma non è ancora terapia standard. È una frontiera scientifica in cui l’innovazione genetica e la medicina dei trapianti si incontrano. Il suo futuro dipenderà dalla capacità di trasformare due esperienze pionieristiche, segnate da fallimenti parziali ma ricche di insegnamenti, in protocolli clinici riproducibili e sicuri.



